医薬品の製造において、製薬会社が自社の設備を使用せず、外部の専門企業に製造を依頼する「受託製造」が一般的になっています。特に近年では、高い技術と品質管理体制を持つCDMO(開発製造受託機関)への委託が進み、効率的かつ安定した供給体制の構築が求められています。
本ページでは、医薬品の受託製造がどのようなフローで行われるのか、実際の製造工程や品質管理、安定供給の観点から詳しく解説します。これからCDMOとの連携を検討している製薬企業担当者の方や、医薬品のサプライチェーンに関心のある方はぜひご参照ください。
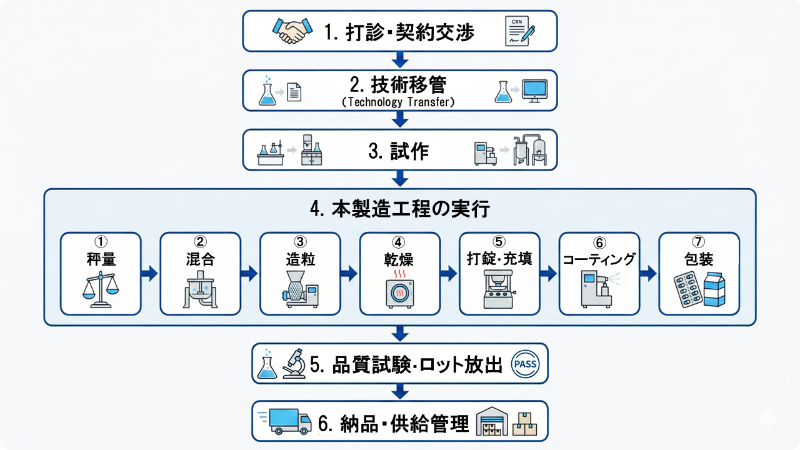
医薬品の受託製造は、製薬会社(委託者)とCDMO(受託者)が契約を交わし、規定された品質・スケジュールに基づいて製品を製造・納品する一連のプロセスです。以下は一般的なフローを示したものです。
このように、受託製造は単なる製造作業の委託ではなく、法令遵守、製造適正、安定供給の3要素が一体となった総合的な連携プロセスです。
医薬品の製造工程は、製剤の剤形(錠剤・カプセル・注射剤など)に応じて異なるものの、GMP(医薬品の製造管理および品質管理の基準)に準拠した一定のプロセスに従って行われます。ここでは、固形製剤(錠剤など)を例に、一般的な製造フローを紹介します。
この工程の中で特に重要なのが、「品質の一貫性」と「交差汚染の防止」です。
医薬品は社会的インフラとしての性質を持つため、計画的かつ継続的な供給体制の確保が求められます。近年ではジェネリック医薬品を中心に供給不安が社会課題となっており、「安定供給の担保」は重要な責務とされています。
平常時からの供給体制強化やリスクマネジメント体制の構築が、CDMO選定・運用の要となります。
製造後の医薬品は、国内外を問わず、必要とされる国や地域へとスムーズに提供できるのがビジネスの理想。CDMOのなかには海外に製造拠点を構え、FDAや三極対応などの認証を得ているところがあり、グローバル展開を考えているのであれば、製造後の支援ができるCDMOに依頼するとよいでしょう。
このサイトではそんなCDMOのなかから、製造したい医薬品の剤形別におすすめのCDMOをご紹介していますので、ぜひ参考にしてみてください。
医薬品の製造は、人々の健康に直結する事業であるため、製品の品質を確保するための厳格な管理体制が不可欠です。特に受託製造では、委託元(製薬会社)と受託先(CDMO)の間での責任範囲や情報共有体制が品質確保に直結するため、厚生労働省も各段階における注意点を示しています。
CDMOは、GMP(Good Manufacturing Practice)に準拠した製造体制を確立していることが前提です。これは、原材料の受け入れから出荷に至るまでの各工程で、品質を担保するための管理基準と手順が確実に運用されていることを意味します。バリデーション(工程・機器・清掃等)の実施と定期的な見直しも必須とされます。
バッチレコードや試験記録、逸脱記録、変更履歴などの品質データを体系的に収集・保管し、委託元企業ともリアルタイムに情報共有できる仕組みを持つことが望まれます。電子化された文書管理システムやLIMS(Laboratory Information Management System)の導入も、効率的な品質管理を支える手段として活用されます。
厚労省の指針では、品質リスクの予見とその制御を重視しています。たとえば、原材料供給元の変更や製造設備の改修といった変更管理(Change Control)を適切に行い、事前にリスクを評価(Quality Risk Assessment)して文書化することが求められます。また、CAPA(是正予防措置)の記録とトラッキングも不可欠です。
CDMOで働くすべての従業員は、業務開始前および定期的に、製造手順・GMP基準・逸脱時の対応方法についての教育訓練を受ける必要があります。教育記録の保存と定期的な理解度評価が推奨され、品質文化を維持するための継続的改善(Kaizen)活動と一体となって運用されます。
製造委託契約の中には、品質管理に関する内容も明文化されている必要があります。たとえば、逸脱が発生した場合の報告体制や、委託元による定期監査の実施条件、変更通知の要件などが契約条項に盛り込まれます。双方向の信頼関係に基づいた連携が、品質不具合の未然防止と早期対応を可能にします。
こうした品質管理体制の構築と運用は、単なる法令順守を超えて、社会的責任と企業価値向上に直結するものです。CDMOを選定する際は、過去の査察結果や監査レポート、品質システムの運用実績などを精査することが推奨されます。
錠剤・カプセルが主の化学合成医薬品や、注射剤・点滴剤が主のバイオ医薬品など、CDMOによって製造できる医薬品に違いがあります。ここではそれぞれのおすすめCDMOについて詳しくご紹介しています。ぜひ自社の開発工程に合った依頼先にお問い合わせください。

| 製造能力 |
|---|
| 錠剤:36億錠/年 細粒・顆粒剤:900t/年 ※ |

| 製造能力 |
|---|
| 公式サイトに記載なし |

| 製造能力 |
|---|
| チューブ:5,500万本 ボトル:2,000万本※ |